Rabu, 29 September 2021
Minggu, 19 September 2021
STRUKTUR ATOM - BILANGAN KUANTUM
STRUKTUR ATOM - BILANGAN KUANTUM
Pada postingan kali ini kita akan membahas tentang Bilangan Kuantum, salah satu bagian dari pembahasan Struktur Atom. Apa sih Bilangan Kuantum itu ? Untuk mengetahui jawabannya silakan lihat dan download di sini.
Semoga postingan ini bermanfaat, dan apa yang menjadi harapan dari pembelajaran lewat postingan ini dapat dicapai.
Posted by Mahmuddin
Jumat, 17 September 2021
SEL ELEKTROKIMIA Part 1 - SEL VOLTA (SEL GALVANI)
SEL ELEKTROKIMIA - SEL VOLTA (SEL GALVANI)
1. Penemu Sel Volta
Sel volta pertama kali ditemukan oleh Alessandro Giuseppe Volta (1745-1827) dan Luigi Galvani (1737-1798). Keduanya ahli kimia Italia.
2. Pengertian Sel Volta
Sel volta adalah sel elektrokimia yang dapat merubah energi kimia (berupa reaksi redoks) menjadi energi listrik (berupa arus listrik).
3. Contoh Sel Volta dalam Kehidupan
4. Rangkaian Sel Volta Klasik
Sebuah sel volta klasik dapat dirangkai seperti gambar berikut :
5. Komponen Sel Volta Klasik
Dari gambar rangkaian sel volta di atas dapat kita lihat, bahwa sel volta klasik tersusun atas komponen-komponen berikut :
- elektroda (berupa lempeng logam, dibedakan menjadi dua, yaitu anoda dan katoda)
- kabel
- bola lampu
- jembatan garam (dibuat dari bahan seperti agar-agar dan KCl)
- larutan elektrolit
6. Mekanisma Kerja Sel Volta
Bagaimana mekanisma kerja sel volta yang dapat menghasilkan arus listrik dari reaksi redoks yang terjadi di anoda dan katoda. Perhatikan gambar berikut.
Jadi arus listrik dihasilkan dari adanya aliran elektron yang berasal dari reaksi oksidasi di anoda menuju katoda.
6. Elektroda dan Potensial Elektroda
Elektroda merupakan lempeng logam yang memiliki potensial elektroda / potensial reduksi yang khas untuk setiap jenis logam.
Elektroda dibedakan menjadi dua, yaitu 1) anoda, elektroda (-) tempat berlangsungnya reaksi oksidasi dan 2) katoda, elektroda (+) tempat berlangsungnya reaksi reduksi.
Potensial elektroda adalah potensial listrik pada elektroda, yang kadang disebut juga potensial ruduksi dan biasanya disimbolkan dengan E0 . Berikut tabel potensial elektroda / potensial reduksi beberapa logam.
Ada beberapa cara menuliskan potensial elektroda/potensial reduksi dari suatu elektroda logam, misal potensial elektroda logam Zn adalah - 0,76 V, untuk ini dapat ditulis sebagai berikut :
1) E0Zn = - 0.76 V
2) Zn2+// Zn, E0 = -0,76 V (menggunakan bagan sel)
3) Zn2+ + 2e- → Zn, E0 = -0,76 V
8. Potensial Sel (Esel)
Setiap sel volta memiliki potensial sel, misalnya baterai, potensial selnya adalah 1,5 V. Lantas apa yang dimaksud potensial sel dan bagaimana cara menghitungnya?
Potensial sel merupakan beda potensial yang ditimbulkan oleh adanya perbedaan harga potensial elektroda / potensial reduksi pasangan anoda ( E0 lebih kecil ) dan katoda ( E0 lebih besar).
Cara menghitungnya adalah dengan mencari selisih antara E0 katoda dengan E0 anoda, yang secara matematis dinyatakan dengan :
Contoh :
Sebuah sel volta tersusun atas elektroda Zn dan Cu seperti pada gambar berikut.
Diketahui :
Zn + 2e- → Zn, E0 = - 0,76 V (E0 lebih kecil) sebagai anoda
Cu + 2e- → Cu, E0 = + 0,34 V (E0 lebih besarl) sebagai katoda,
Maka potensial selnya adalah :
9. Reaksi-reaksi di Anoda, katoda dan Sel
Pada sel volta reaksi redoks terjadi di anoda dan katoda. Di anoda terjadi reaksi oksidasi dan di katoda terjadi reaksi reduksi.
Contoh :
Sebuah sel volta tersusun atas elektroda Zn dan Cu diketahui :
Zn + 2e- → Zn, E0 = - 0,76 V (E0 lebih kecil) sebagai anoda dana) Reaksi di anoda (merupakan reaksi oksidasi), persamaan reaksinya dapat ditulis :
Zn → Zn2+ + 2e-
b) Reaksi di katoda (merupakan reaksi reduksi), persamaan reaksinya dapat ditulis :
Cu2+ + 2e- → Cu
c) Reaksi sel (gabungan reaksi di anoda dan katoda), persamaan reaksinya dapat ditulis :
10. Bagan sel
Cara lain untuk menuliskan persamaan reaksi sel yang diturunkan dari rangkaian sel volta klasik.
Contoh :
Persamaan reaksi sel : Zn + Cu2+ → Zn2+ + Cu
Bagan selnya ditulis : Zn / Zn2+ // Cu2+ / Cu
11. Reaksi Spontan da Tidak Spontan
Pada sel volta reaksi dapat berlangsung spontan dan tidak spontan.
Reaksi berlangsung spontan, jika potensial sel (Esel) = +;
Reaksi berlangsung tidak spontan, jika potensial sel (Esel) = -.
Contoh :
Sebuah sel volta tersusun atas elektroda Zn dan Cu.
Diketahui :
Zn + 2e- → Zn, E0 = - 0,76 V
Cu + 2e- → Cu, E0 = + 0,34 V
Sel volta dibedakan menjadi dua, yaitu :
1) Sel Volta Primer (tak dapat diisi ulang), contoh :
- Baterai
- Alkaline
2) Sel Volta Sekunder (dapat diisi ulang ), contoh :
- Aki Timbal
- Sel Ni - Cd
- Sel Bahan Bakar
REDOKS dan SEL ELEKTROKIMIA Part 2 (Penyetaraan Persamaan Reaksi )
PENYETARAAN PERSAMAAN REAKSI REDOKS
Persamaan reaksi redoks ada yang sudah SETARA dan ada yang BELUM SETARA. Untuk yang BELUM SETARA perlu disetarakan. Bagaimana cara menyetarakannya? Apa saja metode yang digunakan untuk menyetarakan? Apakah suasana reaksi, seperti suasana asam atau suasana basa berpengaruh terhadap penyetaraan?
Untuk menjawab pertanyaan-pertanyaan tersebut , silakan simak tayangan video berikut.
Semoga postingan/pembahasan tentang Penyetaraan Persamaan Reaksi Redoks bermanfaat dan apa yang menjadi harapan dari pembelajaran bisa dicapai.
Posted by Mahmuddin
Senin, 13 September 2021
HUBUNGAN KONFIGURASI ELEKTRON dengan LETAK UNSUR dalam SPU
HUBUNGAN KONFIGURASI ELEKTRON DENGAN LETAK UNSUR DALAM TABEL PERIODIK (SPU)
Tabel Periodik (Sistem Periodik Unsur) sangat erat hubungannya dengan konfigurasi elektron. Bagaimana hubungannya ? Lihat gambar tabel berikut.
Dari tabel di atas terlihat bahwa antara Konfigurasi Eelektron dan letak suatu unsur dalam Sistem Periodik Unsur mempunyai hubungan yang erat. Dengan adanya hubungan ini kita dapat menentukan letak suatu unsur dalam Sistem Periodik Unsur tanpa melihat Sistem Periodik Unsur tersebut. Bagaimana caranya? Caranya adalah dengan :
- menuliskan konfigurasi elektron persubkulitnya lebih dahulu
- kemudian memperhatikan pengisian elektron terakhir di nomor kulit berapa dan subkulit apa berakhir.
- menghitung jumlah elektron pada subkulit terakhir
Catatan :
- nomor kulit, yaitu angka di depan subkulit ini mmenunjukkan PERIODE.
- subkulit menunjukkan apakah unsur tersebut golongan A atau golongan B.
- jika elektron berakhir pada subkulit s atau p berarti golongan A.
- jika elektron berakhir pada subkulit d berarti golongan B
- jika elektron berakhir pada subkult f berarti deret lantanida (4f) dan aktinida. (5f)
- jumlah elektron (jumlah angka pangkat pada subklit terakhir) menunjukkan golongan.
Keempat contoh unsur ini (H, Na, Mg dan Sr) pengisian elektron berakhir pada subkulit s berarti keempat unsur adalah golongan A (golongan utama).
Dua unsur pertama (H dan Na) jumlah elektron terluarnya (jumlah angka pangkat subkulit s ) adalah 1, berarti golongan I.
Dua unsur kedua (Mg dan Sr) jumlah elektron terluarnya (jumlah angka pangkat subkulit s ) adalah 2, berarti golongan II.
Nomor kulit subkulit terakhir untuk H adalah 1, berarti periode 1; untuk Na dan Mg adalah 3, berarti periode 3; dan untuk Sr adalah 5, berarti periode 5.
Kesimpulannya :
Keempat unsur ini dalam Sistem Periodik Unsur masing-masing :
Unsur H terletak pada golongan IA periode 1;
Unsur Na terletak pada golongan IA periode 3;
Unsur Mg terletak pada golongan IIA periode 3;
Unsur Sr terletak pada golongan IIA periode 5.
Secara umum untuk unsur yang pengisian elektronnya berakhir pada subkulit s, rumus penentuan golongan dan periodenya dapat ditulis :
Keterangan rumus : n adalah nomor kulit untuk menentukan perode, dan a jumlah elektron terluar.
2) Penggalan Tabel 1 bagian 2 (tiga unsur kedua : Al, Cl dan Ga)Ketiga unsur ini (Al, Cl dan Ga), pengisian elektron berakhir pada subkulit p berarti ketiga unsur juga adalah golongan A (golongan utama). Akan tetapi jumlah elektron terluarnya ditentukan oleh jumlah elektron subkulit s dan subkulit p (jumlah angka pangkat dari subkulit s dan subkulit p).
Unsur Al, jumlah elektron terluarnya (jumlah pangkat s dan p) adalah 2+1 = 3, berarti golongan III;
Unsur Cl, jumlah elektron terluarnya (jumlah pangkat s dan p) adalah 2+5 = 5, berarti golongan VII;
Unsur Ga, jumlah elektron terluarnya (jumlah pangkat s dan p) adalah 2+1 = 3, berarti golongan III.
Nomor kulit subkulit terakhir untuk Al dan Cl adalah 3, berarti periode 3; dan untuk Ga 4, berarti periode 4.
Kesimpulannya :
Dalam Sistem Periodik Unsur (SPU) masing-masing unsur :
Unsur Al terletak pada golongan IIIA periode 3;
Untuk Cl terletak pada golongan VIIA periode 3;
Untuk Ga terletak pada golongan IIIA periode 4.
Secara umum untuk unsur yang pengisian elektronnya berakhir pada subkulit p, rumus penentuan golongan dan periodenya adalah :
Keterangan rumus : n adalah nomor kulit untuk menentukan periode, a adalah jumlah elektron pada subkulit s dan b adalah jumlah elektron pada subkulit p (jumlah a+b menunjukkan golongan).
3) Penggalan Tabel 1 bagian 3 (Sc, Mn, Pd dan Au)
Keempat contoh unsur ini (Sc, Mn, Pd dan Au), pengisian elektronnya berakhir pada subkulit d , berarti keempat unsur tersebut adalah golongan B. Untuk menentukan golongannya adalah dengan melihat jumlah elektron pada subkulit s dan subkulit d.
Catatan untuk golongan B :
a) Jika jumlah elektron terluar suatu unsur = 8 atau 9 atau 10 maka unsur tersebut termasuk golongan VIII.
b) Jika jumlah elektron terlua suatu unsur = 11 berarti golongan I.
c) Jika jumlah elektron terluar suatu unsur = 12 berarti glongan II.
d) Untuk menentukan periode adalah dengan melihat nomor kulit terbesar (nomor kulit subkulit s).
Unsur Sc, jumlah elektron terluarnya (jumlah pangkat subkulit s dan subkulit d) adalah 2+1 = 3, berarti golongan III dan nomor kulit terbesarnya adalah 4, berarti periode 4:
Unsur Mn, jumlah elektron terluarnya (jumlah pangkat subkulit s dan subkulit d) adalah 2 + 5 = 7, berarti golongan VII dan nomor kulit terbesarnya adalah 4, berarti periode 4;
Unsur Pd, jumlah elektron terluarnya (jumlah pangkat subkulit s dan subkulit d) adalah 2 + 8 = 10, berarti golongan VIII ( bukan golongan X ) dan nomor kulit terbesarnya adalah 5, berart periode 5.
Unsur Au, jumlah elektron terluarnya (jumlah pangkat subkulit s dan subkulit d) adalah 2+9 = 11, berarti golongan I dan nomor kulit terbesarnya adalah 6, berarti periode 6.
Kesimpulan :
Dalam Sistem Periodik Unsur (SPU) :
Unsur Sc terletak pada golongan IIIB periode 4;
Unsur Mn terletak pada golongan VIIB periode 4;
Unsur Pd terletak pada golongan VIIIB periode 5;
Unsur Au terletak pada golongan IB periode 6.
Secara umum untuk unsur yang pengisian elektronnya berakhir pada subkulit d, rumus penentuan golongan dan periodenya dapat dinyatakan :
Keterangan : hurup n berwarna merah untuk menentukan periode.
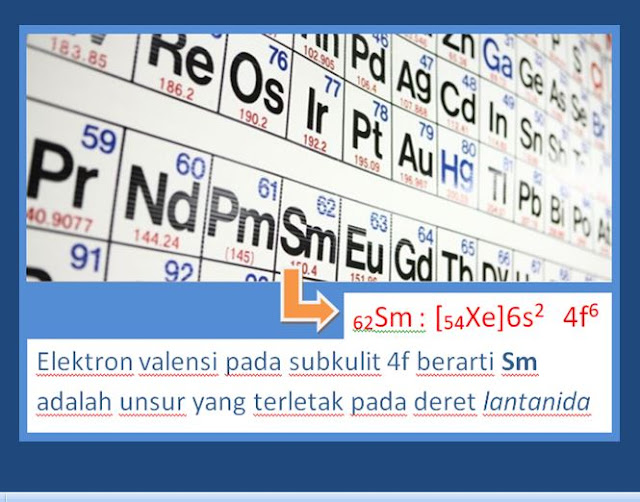
4) Penggalan Tabel 1 Bagian 4 (Sm dan U)
Kedua unsur Sm dan U, pengisian elektronnya berakhir pada subkulit f berarti keduanya termasuk golongan transisi dalam .
Jika pengisian elektron berakhir pada subkulit 4f berarti termasuk deret LANTANIDA;
Jika pengisian elektron berakhir pada subkulit 5f berarti termasuk deret AKTINIDA.
Demikian pembahasan mengenai hubungan konfigurasi elektron dengan SPU.
Semoga bermanfaat dan apa yang diharapkanpada pembelajaran ini bisa dicapai.
Posted by Mahmuddin
Jumat, 10 September 2021
PENGELOMPOKAN UNSUR Part 1
PENGELOMPOKAN UNSUR
Gambar 1 di atas merupakan tabel periodik yang digunakan saat ini. Apa yang kalian lihat dari tabel periodik tersebut? Ternyata unsur-unsur dalam tabel periodik tersebut tersusun dengan aturan tertentu.
Tabel periodik unsur yang ada saat ini mengalami perkembangan mulai dari yang sederhana sampai seperti yang tampak pada gambar 1.
Sekarang timbul pertanyaan :
- Untuk apa unsur-unsur itu dikelompokkan dan disusun?
- Bagaimana tabel periodik unsur itu dapat disusun?
- Apa dasar pengelompokan unsur-unsur dalam tabel periodik tersebut?
1. Sejarah Perkembangan Tabel Periodik Unsur / Sistem Periodik Unsur
Berdasarkan sejarah, semenjak ilmu kimia diperkenalkan oleh para ilmuwan Arab dan Persia, mereka membagi unsur menjadi dua kelompok, yaitu kelompok logam dan nonlogam. Kemudian berkembang dengan Triad Dobereiner, Oktaf Newlands, Tabel Periodik Mendeleev, dan Tabel Periodik Modern.
a) Pengelompokan Berdasarkan Sifat Logam dan Nonlogam
Unsur-unsur yang ada di alam ini ada yang bersifat logam (seperti besi, seng, aluminium, emas, perak, tembaga dan lain-lain) dan ada juga yang bersifat nonlogam (seperti karbon, belerang, phosphor, oksigen, hidrogen dan lain-lain). Oleh karena itu unsur-unsur dikelompokkan menjadi dua golongan, yaitu golongan logam dan golongan nonlogam.
Perbedaan sifat dari kedua golongan tersebut dapat dilihat dari tabel berikut.
b) Triad Dobereiner
Johann Wofgang Dobereiner pada tahun 1829 mengelompokkan tiga unsur yang mempunyai sifat SAMA. Pengelompokan ini disebut TRIAD atau lebih lengkapnya disebut Triad Doberreiner. JW Dobereiner menemukan bahwa dalam satu Triad nomor massa relatif unsur yang terletak di tengah merupakan harga rata-rata nomor massa relatif unsur pertama dan ketiga, seperti tabel di bawah ini :
c) Oktaf Newlands
John Alexander Reina Newlands pada tahun 1864 menyusun unsur-unsur berdasarkan kenaikan massa relatifnya. Dia mendapatkan bahwa unsur yang kedelapan mempunyai sifat yang mirip dengan sifat unsur yang pertama, unsur yang kesembilan mempunyai sifat yang mirip dengan sifat unsur yang kedua, dan seterusnya.
Kelemahan hukum Oktaf Newlands hanya cocok untuk unsur-unsur dengan nomor massa yang kecil dan pengelompokan terlalu dipaksakan.
d) Tabel Periodik Mendeleev
Lothar Meyer dari Jerman dan Dmitry Mendeleev dari Rusia pada tahun 1869 dengan menggunakan prinsip dari Newlands mengadakan penggolongan unsur-unsur berdasarkan nomor massa dan sifat-sifatnya. Mereka berdua di tempat terpisah menghasilkan daftar unsur yang hampir sama.
Menurut Mendeleev, sifat-sifat unsur merupakan fungsi periodik dari nomor massa relatifnya. Perhatikan tabel berikut yang menggambarkan Tabel Periodik Mendeleev.
Kelemahannya adanya unsur yang memiliki nomor massa relatif lebih besar berada di depan unsur dengan nomor massa lebih kecil, contoh Te dengan nomor massa 128 berada di depan I dengan nomor massa 127.
e) Tabel Periodik Modern
Henry Moseley melakukan percobaan untuk menyempurnakan/ memperbaharui Tabel Peridik Mendeleev/Hukum Periodik Mendeleev dan berhasil menyimpulkan bahwa sifat dasar atom suatu unsur adalah nomor atomnya bukan nomor massa relatifnya.
Jadi penemuan Henry Monseley ini menjadi Hukum Periodik Modern yang berbunyi :
Sifat-sifat unsur merupakan fungsi periodik dari nomor atomnya.
Dan digambar seperti pada gambar berikut.
2. Golongan, Perioda dan Blok Pada Tabel Periodik Modern
Kalau kita perhatikan Tabel Peridik Modern di atas bahwa unsur-unsur dikelompokkan ke dalam GOLONGAN dan PERIODA serta BLOK.
a) Golongan
Golongan merupakan pengelompokan unsur-unsur yang memiliki sifat yang sama atau hampir sama dalam kolom dari atas ke bawah (vertikal).
Secara garis besar golongan unsur-unsur dalam Tabel Periodik Modern (Sistem Periodik Unsur/Susunan Berkala Unsur) dibagi menjadi dua, yaitu :
- Golongan A ( Golongan Utama)
- Golongan B ( Golongan Transisi)
- Golongan IA (Golongan Alkali : Li, Na, K, Rb, Cs dan Fr kecuali H )
- Golongan IIA (Golongan Akali Tanah : Be, Mg, Ca, Sr, Ba dan Ra)
- Golongan IIIA (B, Al, Ga, In dan Tl)
- Golongan IVA (C, Si, Ge, Sn, dan Pb)
- Golongan VA (N, P, As, Sb dan Bi)
- Golongan VIA (O, S, Se, Te dan Po)
- Golongan VIIA (Golongan Halogen : F, Cl, Br, I dan At)
- Golongan VIIIA (Golongan Gas Mulia : He, Ne, Ar, Kr, Xe dan Rn)
- Golongan IIIB
- Golongan IVB
- Golongan VB
- Golongan VIB
- Golongan VIIB
- Golongan VIIIB (ada tiga kolom)
- Golongan IB
- Golongan IIB
- Deret Aktinida
- Deret Lantanida
b) Perioda
Periode merupakan pengelompokan unsur-unsur yang memiliki jumlah kulit atom sama dalam lajur dari kiri ke kanan (horizontal) .
Jumlah periode Tabel Periodik Modern (Sistem Periodik Unsur/Susunan Berkala Unsur) ada tujuh, yaitu :
- Periode 1 (ada dua unsur H dan He)
- Periode 2 ( ada delapan unsur Li, Be, B, C, N, O, F dan Ne)
- Periode 3 ( ada delapan unsur Na, Mg, Al, Si, P, S, Cl dan Ar)
- Periode 4 ( ada 18 unsur)
- Periode 5 ( ada 18 unsur)
- Periode 6 (ada 32 unsur, yaitu 18 unsur golongan B + 14 unsur Deret Aktinida
- Periode 7 (Jumlahnya belum pasti masih menunggu penemuan-penemuan baru)
c) Blok
Kemudian unsur-unsur dalam Tabel Periodik Modern, dikelompokkan pula menjadi empat blok, yaitu :
- Blok s, meliputi unsur-unsur golongan IA dan IIA + He
- Blok p, meliputi unsur-unsur golongan IIIA, IVA, VA, VIA, VIIA, dan VIIIA kecuali He
- Blok d, meliputi semua unsur golongan B (Golongan Transisi)
- Blok f, meliputi semua unsur deret Aktinida dan deret Lantanida)
Posted by Mahmuddin
Kamis, 09 September 2021
CONTOH SOAL AKM dan SIMULASI MENGERJAKAN SOAL
CONTOH SOAL AKM (ASESMEN KOMPETENSI MINIMUM) dan SIMULASI MENGERJAKAN SOAL
1. Contoh Soal
1.a. Contoh Soal Literasi (Teks Informasi)
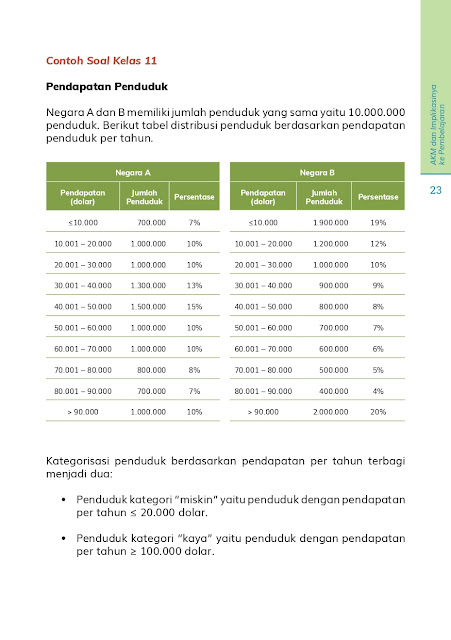
1.b. Contoh Soal Numerasi
2. Simulasi AKM (Literasi Membaca dan Numerasi)
Untuk mencoba simulasi AKM klik di sini. Kemudian pilih dan klik tombol 'AYO COBA AKM' seperti pada gambar berikut.
SELAMAT MENCOBA
Sabtu, 04 September 2021
IMPLIKASI AKM PADA PEMBELAJARAN
IMPLIKASI AKM PADA PEMBELAJARAN
Pada postingan sebelumnya disampaikan bahwa hasil AKM dilaporkan dalam empat kelompok yang menggambarkan tingkat kompetensi yang berbeda, yaitu : 1) Perlu Intervensi Khusus, 2) Dasar, 3) Cakap, dan 4) Mahir.
A. Pemanfaatan Hasil AKM untuk Menguasai Konten : Implikasi Pembelajaran Lintas Mata Pelajaran
1. Contoh Strategi Penguasaan Konten pada Mata Pelajaran IPS
Pelaporan tingkat kompetensi dapat dimanfaatkan guru berbagai mata pelajaran untuk menyusun strategi pembelajaran yang efektif dan berkualitas. Implikasi tingkat kompetensi pada pembelajaran dapat dilihat melalui contoh berikut :
Guru diharapkan memnyesuaikan pembelajarannya sesuai dengan tingkat kompetensi siswa. Berikut contoh strategi pembelajaran yang disesuaikan dengan empat tingkat kompetensi literasi membaca siswa :
1) Siswa di tingkat Perlu Intervensi Khusus belum mampu memahami isi bacaan, siswa hanya mampu membuat interpretasi sederhana. Guru IPS tidak cukup bertumpu pada materi bacaan tersebut. Siswa perlu diberi bahan belajar lain secara audio, visual dan pendampingan khusus.
2) Siswa di tingkat Dasar telah mampu mengambil informasi dari teks, namun tidak memahami secara utuh isi topik koperasi. Siswa dapat diberi sumber belajar pendamping dalam bentuk catatan singkat atau simpulan untuk pemahaman yang utuh.
3) Siswa di tingkat Cakap mampu memahami dengan baik isi teks mengenai koperasi, namun belum mampu merefleksi. Siswa dapat diberi pembelajaran identifikasi kondisi lingkungan siswa, mengaitkan dengan fungsi dan manfaat koperasi.
4) Siswa di tingkat Mahir mampu memahami isi bacaan dan merefleksi kegunaan koperasi dari teks yang diberikan oleh guru. Guru dapat melakukan pembelajaran berupa menyusun beragam strategi pemanfaatan koperasi.
2. Contoh Strategi Penguasaan Konten pada Mata Pelajaran Fisika
Dari contoh ini, diinformasikan empat tingkat kompetensi tindak lanjut yang perlu diberikan:
1) Siswa di tingkat Perlu Intervensi Khusus memiliki penguasaan konsep matematika yang sangat minimal. Siswa ini perlu didampingi mulai dari pencatatan data serta dilakukan diskusi untuk memvalidasi hasil pencatatan data. Diskusi dapat dilakukan dengan teman yang kompetensi numerasinya cakap atau mahir.
2) Siswa di tingkat Dasar sudah menguasai konsep dasar, namun masih kesulitan untuk menerapkan dalam situasi yang relevan. Siswa perlu diberi contoh cara manyajikan data atau menuangkan data hasil catatannya ke dalam bentuk penyajian yang tepat dan akurat. Interpretasi holistik mengenai data sebelum menarik kesimpulan dilakukan dalam diskusi bersama.
3) Siswa di tingkat Cakap mampu memahami konsep dan menerapkan konsepnya, namun perlu diasah kemampuan bernalarnya untuk mengetahui adanya kesalahan pada data atau anomali data. Siswa dapat ditugaskan untuk membandingkan datanya dengan data kelompok lainnya kemudian membuat simpulan umum hasil penelitian dalam satu kelas. Siswa dibimbing dalam menjustifikasi data yang sifatnya anomali.
4) Siswa di tingkat Mahir mampu menerapkan konsep matematika yang dimiliki dalam beragam konteks serta bernalar untuk menyelesaikan masalah. Siswa ini dapat ditugaskan untuk membandingkan data dirinya, data kelompok lainnya dan data dari sumber-sumber lainnya (misal, jurnal ilmiah yang relevan) kemudian membuat generalisasi hasil percobaan yang dilakukan dengan menganalisis beragam data.
B. Pemanfaatan Hasil AKM untuk Meningkatkan Kompetensi Literasi dan Numerasi : Implikasi Pembelajaran Lintas Mata Pelajaran
1. Contoh Strategi Meningkatkan Kompetensi Literasi Membaca pada Mata Pelajaran Seni Budaya dan Prakarya.
Dari contoh ini, diinformasikan empat tingkat kompetensi tindak lanjut yang perlu diberikan:
1) Siswa di tingkat Perlu Intervensi Khusus masih kesulitan memahami resep secara utuh. Siswa diasah kemampuan literasi membacanya tidak hanya dengan membuat cireng, namun juga membuat catatan singkat/rangkuman sederhana mengenai cara membuat cireng berdasarkan resep dari guru.
2) Siswa di tingkat Dasar sudah mampu memahami resep, namun belum memiliki pemahaman yang komprehensif. Siswa pada tingkat ini selain membuat cireng dapat ditugaskan membuat catatan singkat / rangkuman cara membuat cireng yang disertai dengan penanda bagian penting atau bagian yang dapat dimodefikasi pada saat membuat cireng.
3) Siswa di tingkat Cakap sudah memahami secara komprehensif isi resep, namun belum mampu merefleksi dan mengevaluasi. Siswa dapat diberi kebebasan untuk memodifikasi resep / cara membuat cireng, kemudian ditugaskan untuk membuat laporan perbandingan antara cara membuat cireng dengan resep hasil modifikasi dan resep guru.
4) Siswa di tingkat Mahir sudah mampu mengevaluasi dan merefleksi resep guru. siswa tingkat ini sebelum membuat cireng ditugaskan untuk mencari resep cireng lainnya, membandingkan resep-resep, kemudian memutuskan langkah-langkah pembuatan cireng yang akan dijadikan resep untuk dipraktikkan. Hasil telaah beberapa resep tersebut dilaporkan beserta alasan pengambilan keputusan dalam membuat cireng.
2. Contoh Strategi Meningkatkan Kompetensi Literasi Numerasi pada Mata Pelajaran PJOK
Dari contoh ini, diinformasikan empat tingkat kompetensi tindak lanjut yang perlu diberikan:
1) Siswa di tingkat Perlu Intervensi Khusus diberi beberapa contoh hasil pertandingan yang lengkap. Siswa diminta menjabarkan nilai setiap tim dalam satu grup dan menentukan pemenangnya.
2) Siswa di tingkat Dasar diberi contoh hasil pertandingan satu grup yang rumpang dan kondisi pemenang. Siswa diminta menjabarkan kemungkinan hasil pertandingan yang rumpang tersebut.
3) Siswa di tingkat Cakap diberi contoh hasil pertandingan dua grup yang rumpang serta kondisi pertandingan babak selanjutnya. Siswa diminta menjabarkan kemungkinan hasil pertandingan yang rumpang.
4) Siswa di tingkat Mahir diminta mengestimasi kemungkinan pemenang di babak selanjutnya berdasarkan hasil pertandingan empat grup di babak sebelumnya.
Rabu, 01 September 2021
ASESMEN KOMPETENSI MINIMUM (AKM)
ASESMEN KOMPETENSI MINIMUM (AKM) dan Pelaporan Hasilnya
1. Apa itu AKM ?
AKM (Asesmen Kompetensi Minimum) merupakan penilaian kompetensi mendasar yang diperlukan oleh semua siswa untuk mampu mengembangkan kapasitas diri dan berpartisipasi positif pada masyarakat.
2. Ada berapa kompetensi mendasar yang diukur AKM ?
Ada dua kompetensi mendasar yang diukur AKM, yaitu :
1) literasi membaca merupakan kemampuan untuk memahami, menggunakan, mengevaluasi, merefleksikan berbagai jenis teks tertulis untuk mengembangkan kapasitas individu sebagai warga Indonesia dan warga dunia serta dapat berkontribusi secara produktif kepada masyarakat.
2) literasi numerasi (matematika) adalah kemampuan berpikir menggunakan konsep, prosedur, fakta dan alat matematika untuk menyelesaikan masalah sehari-hari pada berbagai jenis konteks yang relevan untuk individu sebagai warga Indonesia dan warga dunia.
Baik pada literasi membaca maupun numerasi, kompetensi yang dinilai mencakup keterampilan berpikir logis-sistematis, keterampilan bernalar dan keterampilan memilah dan mengolah informasi menggunakan konsep dan pengetahuan yang telah dipelajari.
3. Apa yang disajikan oleh AKM kepada siswa ?
AKM menyajikan masalah-masalah dengan beragam konteks yang diharapkan mampu diselesaikan oleh siswa menggunakan kompetensi literasi membaca dan numerasi yang dimilikinya.
4. Apa tujuan AKM ?
5. Apa saja komponen-komponen AKM
6. Apa saja konten literasi membaca dan konten numerasi (matematika)?
Konten literasi membaca dapat berupa :
1) Teks informasi, yaitu teks yang bertujuan untuk memberikan fakta, data, dan informasi dalam rangka pengembangan wawasan serta ilmu pengetahuan yang bersifat ilmiah.
2) Teks fiksi, yaitu teks yang bertujuan untuk memberikan pengalaman mendapatkan hiburan, menikmati cerita dan melakukan perenungan kepada pembaca.
Konten numerasi (matematika) dapat berupa :
1) Bilangan, meliputi representasi, sifat urutan, dan operasi beragam jenis bilangan (cacah, bulat, pecahan,desimal).
2) Pengukuran dan Geometri, meliputi mengenal bangunan datar hingga menggunakan volume dan luas permukaan dalam kehidupan sehari-hari. Juga menilai pemahaman peserta didik tentang pengukuran panjang, berat, waktu dan debit, serta satuan luas menggunakan satuan baku.
3) Data dan ketidakpastian, meliputi pemahaman, interpretasi, serta penyajian data maupun peluang.
4) Aljabar, meliputi persamaan dan pertidaksamaan, relasi dan fungsi ( termasuk pola bilangan) serta rasio dan proporsi.
7. Apa saja proses kognitif literasi membaca dan proses kognitif numerasi matematika ?
Proses kognitif literasi membaca dapat berupa :
1) Menemukan informasi, mencari, mengakses serta menemukan informasi tersurat dari wacana.
2) Interpretasi dan integrasi, memahami informasi tersurat maupun tersirat, memadukan interpretasi antar bagian teks untuk menghasilkan inferensi.
3) Evaluasi dan refleksi, menilai kredibilitas, kesesuaian maupun keterpercayaan teks serta mampu mengaitkan isi teks dengan hal lain di luar teks.
Proses kognitif numerasi dapat berupa :
1) Pemahaman, memahami fakta, prosedur serta alat matematika.
2) Penerapan, mampu menerapkan konsep matematika dalam situasi nyata yang bersifat rutin.
3) Penalaran, bernalar dengan konsep matematika untuk menyelesaikan masalah yang bersifat rutin.
8. Apa saja konteks literasi membaca dan konteks numerasi (matematika) ?
Konteks literasi membaca dan konteks numerasi (matematika) sama, yaitu :
1) Personal, berkaitan dengan kepentingan diri secara pribadi.
2) Sosial Budaya, berkaitan dengan kepentingan antar individu, budaya dan isu kemasyarakatan.
3) Saintifik, berkaitan dengan isu, aktivitas, serta fakta ilmiah baik yang telah dilakukan maupun futuristic.
9. Bagaimana hasil AKM dilaporkan?
Hasil AKM dilaporkan dalam empat kelompok yang menggambarkan tingkat kompetensi yang berbeda. Urutan tingkat kompetensi dari yang paling kurang adalah :
1) Tingkat Kompetensi Perlu Intervensi Khusus,
Pada kompetensi literasi membaca, Tingkat Kompetensi Perlu Intervensi Khusus maksudnya siswa belum mampu menemukan dan mengambil informasi eksplisit yang ada dalam teks ataupun membuat interpretasi sederhana.
Pada kompetensi numerasi, Tingkat Kompetensi Perlu Intervensi Khusus maksudnya siswa hanya memiliki pengetahuan matematika yang terbatas. Siswa menunjukkan penguasaan konsep yang parsial dan kemampuan komputasi yang terbatas.
2) Tingkat Kompetensi Dasar,
Pada kompetensi literasi membaca, Tingkat Kompetensi Dasar maksudnya siswa mampu menemukan dan mengambil informasi eksplisit yang ada dalam teks serta membuat interpretasi sederhana.
Pada kompetensi numerasi, Tingkat Kompetensi Dasar maksudnya siswa memiliki keterampilan dasar matematika: komputasi dasar dalam bentuk persamaan langsung, konsep dasar terkait geometri dan statistika, serta menyelesaikan maslah matematika sederhana yang rutin.
3) Tingkat Kompetensi Cakap
Pada kompetensi literasi membaca, Tingkat Kompetensi Cakap maksudnya siswa mampu membuat interpretasi dari informasi implisit yang ada dalam teks; mampu membuat simpulan dari hasil integrasi beberapa informasi dalam suatu teks.
Pada kompetensi numerasi, Tingkat Kompetensi Cakap maksudnya siswa mampu mengaplikasikan pengetahuan matematika yang dimiliki dalam konteks yang lebih beragam.
4) Tingkat Kompetensi Mahir.
Pada kompetensi literasi membaca, Tingkat Kompetensi Mahir maksudnya siswa mampu mengintegrasikan beberapa informasi lintas teks; mengevaluasi isi, kualitas, cara penulisan suatu teks, dan bersikap reflektif terhadap isi teks.
Pada kompetensi numerasi, Tingkat Kompetensi Mahir maksudnya siswa mampu bernalar untuk menyelesaikan masalah kompleks serta nonrutin berdasarkan konsep matematika yang dimilikinya.
CONTOH SOAL AKM
1. Contoh Soal Literasi Membaca (Teks Informasi)
2. Contoh Soal Numerasi (Matematika)
3. Simulasi AKM Pusmenjar Kemdikbud
Untuk mencoba simulasi soal AKM Pusmenjar Kemdikbud klik di sini
KISI KISI SOAL KIMIA UJIAN SEKOLAH 2024
KISI KISI SOAL KIMIA UJIAN SEKOLAH 2024 Siswa dapat menyebutkan : 1. Tanda-tanda terjadinya suatu reaksi kimia 2. Menen...
-
HUBUNGAN KONFIGURASI ELEKTRON DENGAN LETAK UNSUR DALAM TABEL PERIODIK (SPU) Tabel Periodik (Sistem Periodik Unsur) sangat erat hubungannya ...
-
PENYETARAAN PERSAMAAN REAKSI REDOKS Persamaan reaksi redoks ada yang sudah SETARA dan ada yang BELUM SETARA . Untuk yang BELUM SETARA pe...
-
SEL ELEKTROKIMIA - SEL VOLTA (SEL GALVANI) 1. Penemu Sel Volta Sel volta pertama kali ditemukan oleh Alessandro Giuseppe Volta (1745-1827) ...